Mais revisões atualizadas da doença celíaca, osteoporose e osteopenia
Continuando aos avanços desta revisão: Clique aqui
Seguem as atuais: Aqui até 2010
Esta Atual de 2015 : Aqui
Tradução google abaixo atualizada:
Seguem as atuais: Aqui até 2010
Esta Atual de 2015 : Aqui
Tradução google abaixo atualizada:
Ossos da Contenção: recuperação da densidade mineral óssea na doença celíaca - uma revisão sistemática
Recebido: 19 de janeiro de 2015 / Aceito: 26 de março de 2015 / Publicado: 7 de maio de 2015
Abstrato
: A doença óssea metabólica é uma co-morbidade freqüente em adultos recém-diagnosticados com doença celíaca (CD), uma doença auto-imune desencadeada pela ingestão de glúten dietético. Esta revisão sistemática de estudos analisou a eficácia da dieta isenta de glúten, atividade física, suplementação de nutrientes e bisfosfonatos para o baixo tratamento da densidade óssea. O controle de casos e os projetos de coorte foram identificados a partir de PubMed e outros bancos de dados acadêmicos (de 1996 a 2015) que observaram adultos recém-diagnosticados com CD durante pelo menos um ano após o tratamento dietético usando a análise de absorciometria de raios-x de energia dupla (DXA). Apenas 20 dos 207 estudos preencheram os critérios de inclusão. A qualidade metodológica foi avaliada utilizando a lista de verificação da Declaração de Relatórios de Estudos Observatórios em Epidemiologia (STROBE). A aderência à dieta sem glúten resultou em recuperação parcial da densidade óssea em um ano em todos os estudos e recuperação total no quinto ano. Não foram observadas diferenças de tratamento entre a dieta isenta de glúten sozinha e dieta mais bisfosfonatos em um estudo. Para pacientes malnutridos, a suplementação com vitamina D e cálcio resultou em melhora significativa. A evidência do impacto da atividade física na densidade óssea foi limitada. As estratégias terapêuticas destinadas a modificar fatores de estilo de vida ao longo da vida útil devem ser estudadas.
Palavras-chave:
doença celíaca; glúten; Osteoporose; dieta; atividade física; Densidade óssea; Deficiência de nutrientes1. Introdução
A doença celíaca (CD) é desencadeada em indivíduos geneticamente suscetíveis pelo glúten dietético que resulta em dano intestinal e ocorre em 1% da população na Europa e nos Estados Unidos [ 1 ]. Aproximadamente 75% dos pacientes recentemente diagnosticados com doença celíaca apresentam baixa densidade mineral óssea (DMO). E quando comparados por idade e sexo a uma população não afetada, os pacientes celíacos têm um risco 40% maior de fratura óssea [ 2 ]. Mesmo com uma apresentação silenciosa ou extra-intestinal, como dermatite herpetiforme ou demência, freqüentemente é encontrada baixa massa óssea [ 3 , 4 , 5 ]. Um terço dos casos recém-diagnosticados têm mais de 60 anos de idade que coincide com um período de risco aumentado de quedas apenas piorou pela presença de comorbidades [ 6 , 7 ]. As mulheres com doença celíaca têm uma taxa muito maior de fraturas durante o período de 10 anos antes do diagnóstico e 5 anos depois [ 8 ]. Os efeitos cumulativos da inflamação induzida pelo glúten, atraso do tratamento e má absorção resultam em menor densidade óssea e fragilidade óssea.
O tratamento mais efetivo para a doença celíaca e comorbidades relacionadas, a dieta sem glúten (GFD), é sem disputa na literatura.No entanto, as melhorias na DMO após o tratamento podem levar até dois a cinco anos após a recuperação da mucosa [ 9 , 10 , 11 , 12]. As deficiências nutricionais são comuns durante o ano inicial do tratamento para a doença celíaca, mas há pouco conteúdo no estado de micronutrientes adultos E densidade mineral óssea nesta população além do estado de cálcio e vitamina D [ 13 , 14 , 15 , 16 ].
O objetivo desta revisão sistemática é examinar se um GFD, sozinho ou em combinação com outras intervenções, leva à recuperação mineral óssea em adultos recém-diagnosticados com doença celíaca. Um segundo objetivo é identificar lacunas na literatura que informariam o desenho de futuros ensaios clínicos e estudos de intervenção em saúde.
2. Métodos
2.1. Critérios para considerar estudos para esta revisão
A pesquisa bibliográfica foi limitada aos artigos de língua inglesa sobre adultos tratados e tratados com doença celíaca observada durante um ano ou mais. Estudos que eram exclusivamente silenciosos ou assintomáticos foram incluídos se fossem parte da amostra devido ao seu estado mineral ósseo conhecido. Os tipos de estudos considerados foram coorte, controle-caso e projetos controlados randomizados. O relatório do caso ea série de casos foram excluídos da análise. Estudos que incluíram condições co-mórbidas, como diabetes ou hiperparatireoidismo primário, foram excluídos. Foram procurados ensaios controlados randomizados e intervenções que identificaram a dose, a frequência, o tipo de suplementação nutricional e a atividade física.
2.2. Estratégia de Pesquisa para Identificação de Estudos
Uma pesquisa por palavra-chave foi realizada em PubMed (janeiro de 1996 a abril de 2015); Embase; CINAHL plus texto completo;EBSCO; Scopus; Dissertações e teses de ProQuest e recursos da biblioteca da Universidade de Connecticut (HOMER). As palavras-chave da estratégia de pesquisa MEDLINE foram "doença celíaca" [MeSH]) E ("densidade mineral óssea" OU "osteoporose" OU "densidade óssea") E ("exercício" OU "atividade física") E ("nutrição" OU "glúten" -free ") no título da publicação, resumo ou texto completo. Os critérios de inclusão para este esforço foram estudos com foco no tratamento de adultos recém-diagnosticados com doença celíaca que relataram a variável dependente como densidade mineral óssea (DMO) como um T-score de absorciometria de raios-X de dupla energia (DXA) na linha de base E na avaliação anual. As modalidades de tratamento procuradas incluíam dieta sem glúten, atividade física ou suplementação de vitaminas e minerais. Estudos de caso e documentos que não relataram dados DXA na linha de base foram excluídos.
As listas de referência de artigos chave foram pesquisadas manualmente no banco de dados Cochrane de revisões sistemáticas, meta-análises e artigos de revisão, bem como artigos em (Osso, Gut, Osteoporose Internacional e American Journal of Gastroenterology).Finalmente, foram revisados artigos de revisão de revistas e meta-análises para estudos não celíacos de baixa DMO.
2.3. Avaliações de qualidade
Os testes clínicos que atendem aos critérios estão listados na Tabela 1 . A qualidade metodológica foi avaliada utilizando as recomendações STROBE (Fortalecimento do Relato de Estudos Observacionais em Epidemiologia) usando listas de verificação separadas para resumos de conferências, estudos de controle de casos, estudos de coorte e estudos transversais [ 17 ]. O uso de uma avaliação qualitativa utilizando um sistema de porcentagem para categorizar os estudos propostos por outros autores revelou-se não razoável devido à idade de alguns dos trabalhos, publicado anos antes das recomendações do STROBE [ 18 ]. O sistema final utilizado foi uma combinação de STROBE (50% -80% preenchido) e se faltamos itens deixaram o leitor questionando critérios de elegibilidade ou viés nos resultados relatados. Após 2008, a maioria dos artigos caiu na categoria de qualidade "A".
2.4. Visão geral dos estudos
Três categorias de estudo foram identificadas: GFD; GFD e suplemento nutricional; GFD e bisfosfonatos; E uma combinação de GFD, suplemento e exercício físico. As medidas de resultado em artigos selecionados incluíram: DXA (pescoço femoral, trocânter e coluna lombar), ligando do ativador do receptor da relação NFκB (RANKL) / osteoprotegerina (OPG), adesão a um GFD e nível de atividade física. Os testes clínicos que atendem aos critérios estão listados na Tabela 1 .
3. Resultados
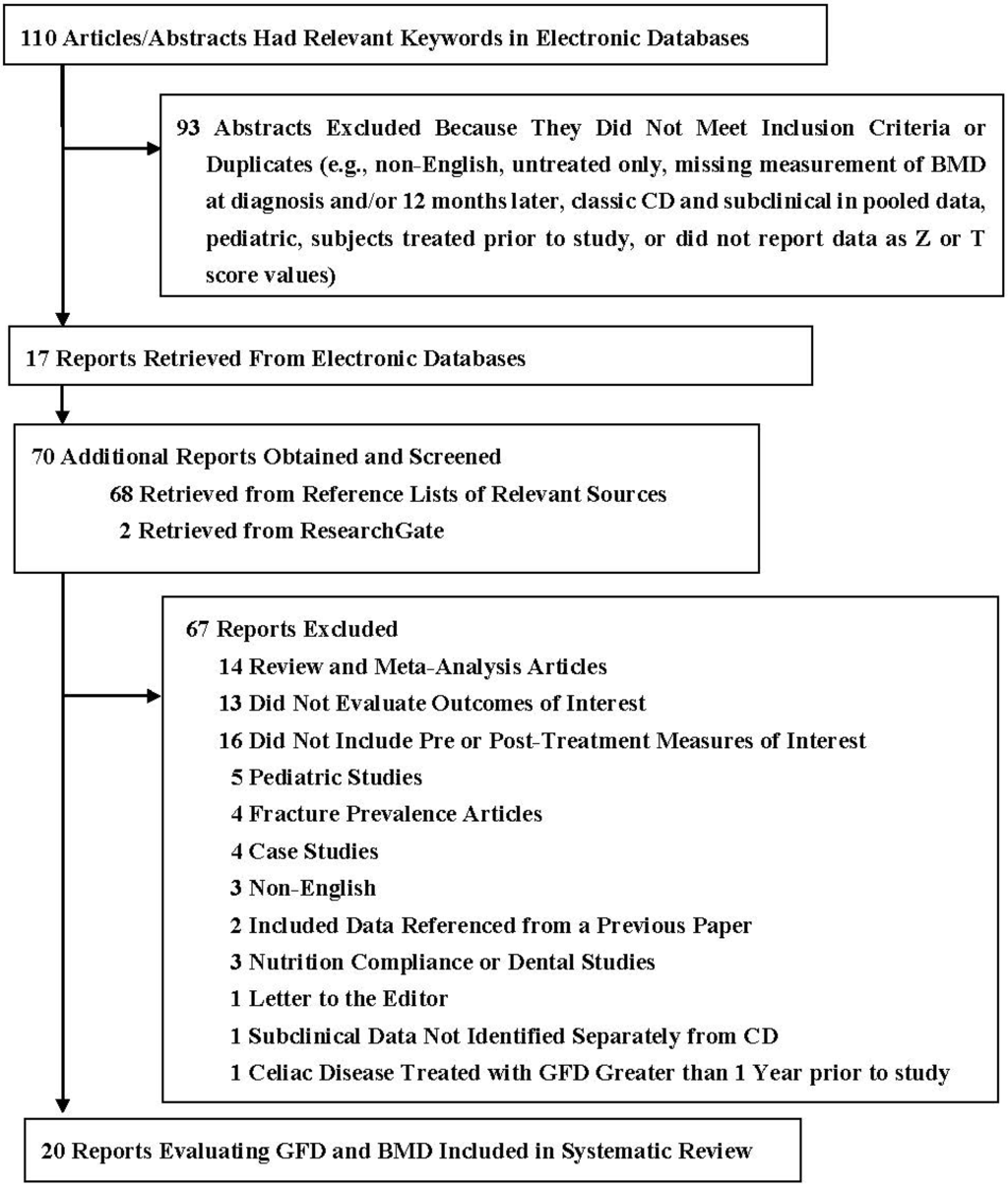
Após a triagem inicial de artigos e resumos da estratégia de busca inicial, foram recuperados um total de 180 artigos. O processo sistemático gerou 20 relatórios ( Figura 1 ). Durante o período desta revisão, houve uma evolução no diagnóstico e classificação de CD com maior aceitação dos resultados do teste de sorologia para triagem e monitoramento em adultos, combinada com biópsia para diagnóstico [ 19 , 20 , 21 ]. Esses desenvolvimentos tornaram as comparações do estudo mais difíceis devido à heterogeneidade clínica entre indivíduos com pouca ou nenhuma atrofia vilosa.
Vários testes são usados para medir a densidade óssea, incluindo o DXA, tomografia computadorizada quantitativa (QTC), absorciometria de fótons e ultra-som. A perda mineral de osso adulto é categorizada em osteopenia e osteoporose. A Organização Mundial da Saúde (OMS) estabeleceu a DXA como a melhor técnica de densitometria para a medição da densidade óssea em mulheres pós-menopáusicas, mas a sensibilidade da DXA é menor em relação à QTC em indivíduos com doença celíaca [ 41 ]. Um índice T entre -1 e -2,5 e ≤2,5 indica perda mineral óssea com maior risco médio de fratura [ 12 ]. Vários fatores de risco e os resultados da análise DXA são bons preditores de risco relativo de fratura, e a previsão é reforçada quando as comorbidades, como a doença celíaca, são adicionadas ao índice FRAX (WHO Fracture Risk Assessment Tool) [ 42 ].
3.1. Terapia Dietética
Os estudos analisados que relataram uma medida de conformidade dietética demonstraram que a adesão ao GFD tem um efeito positivo na densidade mineral óssea [ 4 , 36 , 38 , 43 ]. O maior ganho de tratamento dietético ocorre no primeiro ano de estudos longitudinais que seguiram indivíduos por mais de 12 meses [ 27 , 34 , 37 ]. Mas a recuperação total para adultos foi alcançada principalmente após 5 anos [ 27 ]. Os adultos mais velhos, recentemente diagnosticados, se beneficiam do GFD com ganhos significativos na coluna vertebral e lombar sendo relatados no primeiro ano de tratamento [ 35 , 36 ]. A desnutrição associada à malabsorção atrasou a restauração da DMO em um grupo de alto risco de vitamina D e suplemento de cálcio, enquanto indivíduos com menos comprometimento nutricional no mesmo estudo evoluíram de osteoporose para osteopenia em um ano de tratamento [ 33 ]. Os marcadores de rotatividade óssea Interleukin-18 (IL-18), Interleukin-6 (IL-6) e Telopeptídeo N- terminal de procollagen tipo I foram medidos em indivíduos tratados ( n = 25), não tratados ( n = 17) e controles ( N = 21) [ 30 ]. O grupo GFD apresentou níveis reduzidos de IL-18 e uma razão menor de RANKL / osteoprotegerina (OPG) em comparação com indivíduos não tratados, enquanto o tetrapéptido N- terminal de procollagen tipo I era comparável aos controles. Outro estudo analisou a regulação da osteoclastogênese e do turnover ósseo na doença celíaca em um estudo de coorte de mulheres saudáveis pré-menopáusicas e indivíduos compatíveis com a doença celíaca que não apresentavam evidência de hipoparatiroidismo [ 44 ]. Os autores relataram que a relação OPG / RANKL foi significativamente menor nos pacientes com CD do que nos controles (14,8 ± 6,9 versus 19,4 ± 9,2; p <0,05).
Em geral, os estudos mostraram que um GFD para a maioria dos pacientes é uma terapia eficaz para a recuperação mineral óssea a longo prazo. O uso de medidas intermediárias, como DMO, qualidade de vida e rooteamento ósseo, é mais prático do que as estimativas de redução de fraturas, pois esses estudos seguiram pacientes por um a cinco anos. A incidência de fraturas em um grupo de participantes compatíveis com dieta ( n = 265, M / F = 422/223) antes e 5 anos após o diagnóstico foi comparada a uma coorte de pacientes com transtornos gastrointestinais funcionais ( n = 530, M / F = 84/446) [ 45 ]. A incidência de fraturas diminuiu após o tratamento (Taxa de Incidência (IR) = -1,22 eventos por 1000 pacientes ano -1 ) e Risco de Saúde (FC) da fratura foi comparável aos controles (HR: 1,28, IC 95%: 0,74-2,21, p = Ns), confirmando assim o benefício a longo prazo do GFD.
3.1.1. GFD e suplementação de nutrientes
A revisão identificou 3 artigos que abordaram os efeitos do tratamento da suplementação de vitaminas e minerais na DMO [ 25 , 26 , 33 ]. A abordagem de Ciacci, et al. Era um constante teor de cálcio na dieta de 1250 mg diariamente com dieta isolada ou a adição de um suplemento para aqueles que eram intolerantes à lactose [ 25 ]. Não houve alteração significativa na vitamina D, aumento do cálcio urinário e aumento significativo da DMO na coluna lombar, no pescoço femoral e no triângulo de Ward neste estudo. Os não respondedores eram mais propensos a ser mais velhos e menopausa. Mautalen e associados randomizaram participantes para uma condição de dieta sem glúten ( n = 7) ou dieta mais cálcio (1,0 g dia -1 ) e vitamina D (32,000 UI semana -1 ) ( n = 7) [ 26 ]. Os resultados deste teste foram comprometidos pela não conformidade. Os indivíduos aderentes tiveram ganhos significativos na DMO em comparação aos pacientes que com lapsos freqüentes, e a melhoria favoreceu o axial em relação ao esqueleto periférico. Por fim, Papamichael, et al. Observou soro 25 (OH) D 3 , hormônio paratireóide (PTH) e cálcio antes e depois do tratamento [ 33 ]. Apenas mulheres com má absorção severa receberam suplementos, o resto do grupo de estudo dependia do GFD e da luz do sol. Em resumo, o efeito da suplementação depende da gravidade da doença no diagnóstico e exposição ambiental à radiação UV. A DMO da maioria dos pacientes melhorou significativamente a vitamina D e cálcio adequados no primeiro ano.
Satenga-Guidetti, et al. Avaliou o estado nutricional pré e pós-tratamento dos indivíduos ( n = 86) em um GFD sem suplementação com folato sérico, 25OH-D, hemoglobina, transferrina e medição de albumina, bem como cálcio urinário [ 29 ]. Os pesquisadores observaram após um acompanhamento de um ano que 34% dos 86 pacientes recém-diagnosticados tinham uma densidade mineral óssea normal, enquanto 40% tinham osteopenia e 26% de osteoporose com tratamento dietético. Não houve diferenças entre gênero nos marcadores do metabolismo ósseo ou a maioria dos índices nutricionais. A única diferença foi entre mulheres pré e pós-menopausa, onde DMO e vários marcadores metabólicos ósseos foram significativamente diferentes. Isso contrasta com outro estudo em que a DMO reduzida foi encontrada após a cicatrização completa das lesões duodenais em metade da amostra do paciente [ 46 ]. Os pesquisadores concluíram que medidas adicionais além da conformidade e aconselhamento alimentar devem ser levadas em consideração para aumentar a DMO.
A falha no tratamento pode realmente ser o resultado de um GFD altamente processado, pois está associado ao crescimento excessivo de bactérias do intestino delgado (SIBO) [ 47 ]. Foi demonstrado que um GFD altamente processado altera o microbioma intestinal e aumenta os sintomas de GI, o que leva a uma maior permeabilidade da barreira epitelial em pacientes com CD [ 48 , 49 , 50 ]. A saúde da microbiota intestinal e os sintomas relacionados à normalização do impacto do metabolismo ósseo no SIBO. O GFD não reduz o risco de co-morbidades graves, como adenocarcinoma do intestino delgado, linfoma de células T associadas à enteropatia (EATL), abortos, infarto do miocárdio, adenocarcinoma do colo, linfoma MALT gástrico, nejuno-ileite ulcerativa, colangite grave Hepatite não alcoólica e trombocitopenia autoimune [ 51 ].
O estado nutricional no momento do diagnóstico, a idade, o estado da menopausa, o meio ambiente e a conformidade com a dieta moderam o efeito dos suplementos dietéticos na DMO. Existe controvérsia quanto à quantidade de suplementação necessária para reverter a desnutrição para os principais nutrientes. Um ensaio clínico grande que compara a constante vitamina D e a abordagem dietética de cálcio a uma GFD sem suplementação é necessária. Como a manutenção da vitamina S sérica é melhorada na presença de ingestão de cálcio adequada e altos níveis de atividade física, o estudo deve coletar medidas diretas da exposição total à radiação UV e atividade física [ 52 ].
3.1.2. GFD e Bisphosphonates
O uso de terapia de reposição hormonal ou bifosfonatos, foi demonstrado em mulheres pré e pós-menopausa saudáveis para serem eficazes na restauração da massa óssea; E os dados sugerem que combinar essas terapias com exercício com peso pode ter efeitos aditivos [ 53 , 54 ]. Um pequeno estudo piloto ( n = 28) que tratou pacientes com CD com GFD e ácido zoledrônico, ou um GFD suplementado com cálcio e colealciferol relataram que não houve diferença significativa na eficácia [ 39 ]. A replicação deste estudo com um tamanho de amostra maior que inclui adultos mais velhos pode ser mais representativa da população de CD adultos.
3.1.3. GFD e atividade física
Poucos pesquisadores estudaram o efeito da atividade física sobre a densidade óssea nesta população. Passananti e associados estudaram dois grupos de mulheres (20-60 anos) e compararam as medidas de linha de base para o Questionário Internacional de Atividade Física (IPAQ), escala analógica visual de fadiga (VAS), complicações dietéticas, sintomas gastrointestinais, vitamina D sérica, anti-transglutaminase Anticorpos (U mL -1 ) e DMO em coortes de seguimento de 2 ou 5 anos [ 37 ]. As mulheres que tomavam contraceptivos orais ou terapia de reposição hormonal foram excluídas. Um total de 110 participantes foram matriculados no estudo, mas 15 foram perdidos no seguimento ou não aderiram ao GFD. O tamanho final da amostra das duas coortes foi n = 48, n = 47, para as coortes de seguimento de 2 e 5 anos, respectivamente. As medidas de DMO foram realizadas no fêmur direito e na coluna lombar. Os testes de qui-quadrado foram usados para dados categóricos e ANOVA para medidas contínuas. A DMO de linha de base e de seguimento (FU) foi analisada por t-testes de duas amostras e pares, com um intervalo de confiança definido em 95%. As medidas de saúde também incluíram IMC, patologia do intestino delgado usando categorias Marsh para comparações de lesões e idade de menarca e menopausa. No grupo FU de 2 anos, 53,7% dos participantes relataram baixa atividade física e 10,6% eram altamente ativos (IPAQ = 3). Comparado com a fadiga basal neste grupo, não houve diferença estatística. O grupo FU de 5 anos foi mais ativo, com 46,3% relatando níveis baixos e 14,6% altamente ativos. No entanto, os sujeitos ativos neste grupo provavelmente apresentaram fadiga ( p = 0,039 post hoc ). O índice médio de IPAQ para ambos os grupos não foi significativamente diferente (1,60 ± 0,67 vs 1,87 ± 0,88; p > 0,05). Não houve diferença significativa entre os grupos na FU para DMO e sem relação entre DMO e intensidade da atividade física (PA) ( p > 0,05 na coluna lombar e fêmur proximal). Os pesquisadores concluíram que a atividade física tem um papel menor no apoio à recuperação mineral óssea em pacientes celíacos. É importante notar que os participantes do estudo tiveram níveis normais de vitamina D, mas não atenderam às suas necessidades dietéticas de cálcio.
Di Stefano (2000) observou fatores de estilo de vida em pacientes não tratados com CD e DMO [ 55 ]. Os participantes ( n = 39) foram retirados de um grupo de pacientes consecutivos com um espectro de transtornos sensíveis ao glúten: celíaco clássico, dermatite herpetiforme, subclínico ou refratário (não responsivo). As variáveis independentes foram gênero, status de tabagismo, gravidade dos sintomas, duração do sintoma, exposição à luz solar e nível de atividade física. O nível de PA foi determinado por auto-relato de atividades ocupacionais, recreativas (ciclismo e caminhada rápida) e atividades da vida diária em uma escala de freqüência de 0-4 [ 56]. Os preditores da DMO eram gênero, desnutrição, gravidade e PA. A gravidade dos sintomas previu baixa DMO no pescoço lombar e femoral (-2,5 ± 0,8, p <0,001). A PA foi correlacionada com DMO na região lombar ( r = 0,57, p <0,004) e femoral ( r = -0,71, p<0,004); E o conteúdo mineral ósseo (BMC) foi correlacionado com BMC lombar ( r = 0,59, p <0,001) e BMC femoral ( r = 0,58, p<0,001).
Os estudos concordam que a fadiga e os sintomas celíacos afetam a freqüência e a intensidade do exercício. As medidas de resultado, sejam bioquímicas ou radiológicas, não levam em consideração a força muscular ou a flexibilidade. Nenhuma medida direta de nível de aptidão ou movimento de todos os dias foi publicada. Além de um estudo de Gonzalez et al. [ 57 ], poucos artigos identificaram alterações globais na composição corporal, apesar das observações de que o tratamento resulta em obesidade em alguns pacientes [ 58 , 59 ]. Em idosos, o impacto do exercício nas vias bioquímicas envolvidas no remodelamento ósseo, como o ativador do receptor do fator nuclear κB (RANK) / RANKL / OPG, é positivo e particularmente responsivo a tipos específicos de exercício (por exemplo, exercícios de alto ou baixo impacto E treinamento de resistência) [ 60 ]. Observou-se que os indivíduos com CD têm uma relação alterada de osteoprotegerina / RANKL, que também pode predispor os pacientes a doenças cardiovasculares [ 44 , 61 ] A futura pesquisa de intervenção em saúde em doença celíaca deve se concentrar na melhoria do bem-estar, força e capacidade funcional nesta população .
Um estudo randomizado, em dupla ocultação versus placebo paralelo sobre a eficácia da l- carnitina na fadiga em pacientes com doença celíaca [ 62 ]. Os participantes receberam um placebo ou 2 g de l- carnitina diariamente durante 180 dias. A it-carnitina desempenha um papel importante na contração muscular e na produção de energia. O grupo experimental experimentou um aumento no transportador de catiões orgânicos 2 (OCTN2), um transportador dependente de sódio para carnitina que facilita a absorção de carnitina, bem como as aminas, algumas vitaminas. O grupo de tratamento de l- carnitina relatou melhora significativa na fadiga, conforme avaliado pela escala VAS. O aumento da OCTN2 pode explicar essa mudança. Em última análise, baixos níveis de atividade física em pessoas com CD podem ser melhorados através do tratamento de l- carnitina, o que pode auxiliar na estimulação da deposição mineral óssea.
O tipo específico de exercício pode ser um fator crítico para melhorar a saúde óssea. Marques e associados estudaram o efeito da resistência e protocolos de treinamento de aeróbica de impacto moderado na DMO do fêmur proximal, força muscular, equilíbrio, composição corporal, níveis séricos de OPG e RANKL em mulheres mais velhas ( n = 71). Após oito meses da intervenção, apenas o grupo de treinamento de resistência experimentou mudanças positivas na DMO e força muscular [ 63 ]. Ambos os protocolos tiveram efeitos significativos no controle do equilíbrio funcional, um fator chave na prevenção de queda. Um estudo posterior deste autor observou o efeito do treinamento de impacto combinado para equilíbrio e força muscular nas extremidades inferiores em homens e mulheres; Os pesquisadores relataram melhora no equilíbrio dinâmico (6,4%), força muscular (11,0%) e trocânter (0,7%), intertrocantro (0,7%), hipérostas totais (0,6%) e DMO da coluna lombar (1,7%), enquanto a osteocalcina, Os níveis de OPG e RANKL permaneceram inalterados [ 64 ]. O exercício realizado com dose e intensidade adequadas aborda múltiplos fatores de risco para osteoporose e fraturas.Pesquisas adicionais sobre a intervenção do estilo de vida da doença celíaca devem começar com barreiras conhecidas à PA e terapias motivacionais em outras populações [ 65 ].
3.1.4. Deficiências Nutricionais, Sódio Dietético, Disbiose e Inflamação
A suplementação de folato é um tratamento eficaz para homocisteína elevada em CD [ 66 ]. B12 e deficiência de ferro é um sintoma comum no CD não tratado e em um estudo foi descoberto em 41% dos participantes [ 67 ]. Dahele e Ghosh relataram que após a administração oral e parentérica de B12, todos os pacientes ( n = 39) apresentaram níveis séricos normais de B12 ao seguimento de um ano. Um novo papel para o B12 na saúde óssea foi demonstrado em um modelo de ratinho de deficiência de B12 demonstrando que a deficiência prejudica a síntese de taurina e melhora a síntese de IGF-1 dependente do hormônio do crescimento no fígado; Isto aumenta a função dos osteoblastos ( Figura 1 ) [ 68 ]. A pesquisa em seres humanos deve se concentrar na reavaliação dos requisitos de vitamina B12 em CD para determinar seu papel na remineralização óssea.
A microbiota intestinal tem sido implicada no desenvolvimento de CD que pode não ser corrigido após o tratamento. Devido ao baixo nível de phylum Bacteroides e abundância de Firmicutes nas fezes de pessoas com CD, esse desequilíbrio tem um efeito pró-inflamatório ao aumentar a citocina de IL-10 [ 69 ]. O GFD não normalizou as bactérias intestinais em um estudo de seguimento de dois anos com crianças com CD e demonstrou induzir a disbiose em adultos saudáveis alimentados com uma dieta isenta de glúten por um mês [ 50 , 70 ]. O metabolito de vitamina D 25 (OH) 2D3 foi demonstrado em um estudo in vitro para estimular células dendríticas para induzir células T reguladoras (Treg) [ 71 ]. Nesse estudo, os resultados mostraram que a IL-10 derivada de células dendríticas dérmicas induzem células TR1-IL-10 +. A microbiota intestinal também afeta a diferenciação de células T e a susceptibilidade do hospedeiro a doenças autoimunes [ 72 ]. O gênero Bifidobacterium é baixo nas fezes de pacientes celíacos em um GFD em comparação com controles saudáveis que consomem uma dieta regular. Este gênero foi mostrado para proteger contra inflamação e danos nas mucosas causados por péptidos de gliadina in vitro [ 73 ].
Uma mudança na dieta pode trazer melhora a longo prazo na inflamação crônica e na má absorção de nutrientes devido a alterações no microbioma intestinal [ 74 ]. A função de barreira melhorada devido à dieta e à atividade física foi mostrada em um estudo de jogadores de rugby de elite profissionais comendo uma dieta rica em proteínas, plantas e vegetais de soro de leite durante o campo de treinamento [ 75 ]. O DNA das amostras fecais mostrou uma rica diversidade de organismos como o filo Firmicutes, o gênero Akkermansia e menos Bacteroides do que em dois grupos de controles menos ativos, compostos por peso normal e indivíduos obesos.
A conclusão de uma análise multivariada de fatores que prevêem a recuperação em 30 mulheres e 11 homens com CD como gênero (mulheres), idade de pré-tratamento e pré-tratamento de DMO predizem independentemente mineralização óssea, especialmente na coluna lombar [ 25 ]. O coeficiente de regressão da DMO da coluna lombar (+0,060 a +0,160 g cm -2 ) não se sobrepôs ao intervalo de confiança de 95%. Os autores identificaram em sua discussão que a suplementação de vitamina D 3 pode ser um fator importante que não foi abordado em seu estudo. Em um estudo duplo cego controlado com placebo, Fickling e associados (2001) administraram 300.000 unidades de choicecalciferol (vitamina D) por injeção intramuscular ou placebo salino a pacientes recentemente diagnosticados com CD [ 76 ]. Os dados foram coletados aos 6, 12 e 24 meses. Ambos os grupos viram melhorias na DMO, mas nenhuma diferença significativa foi encontrada entre os grupos.
Um relato de caso de uma mulher com perda mineral óssea grave ilustra a necessidade de tratamento individualizado de CD [ 14 ].Uma mulher sedentária de 37 anos diagnosticada com CD apresentou inicialmente uma DMO baixa e recebeu cálcio (1000 mg dia -1 ) e vitamina D (400 UI dia -1 ). Após um ano, uma Dietista Registrada-Nutricionista verificou a conformidade com a dieta, a vitamina D sérica permaneceu baixa (33 nmol L -1 ), e a dose foi posteriormente aumentada para 1000 UI dia -1 . Após um aumento de 81% na coluna vertebral e uma alteração de 60% no quadril no ano 3, sua massa óssea estabilizou até o ano 4. Isso demonstra a necessidade de avaliar o estilo de vida, nutrição e estado ósseo ao longo do tratamento.
Um estudo de 10 anos de indivíduos com CD relatou que mais da metade sofria de deficiências vitamínicas em folato, B12 e B6, como evidenciado por níveis elevados de homocisteína, baixo folato plasmático e B6 [ 77 ]. Em um estudo holandês de adultos recém-diagnosticados ( n = 80), pesquisadores observaram deficiências em vitamina A, B6, ácido fólico, B12 e zinco em 67% dos participantes [ 78 ]. B12 e deficiência de ferro são comuns em CD não tratados e em um estudo foi descoberto em 41% dos participantes [ 67 ]. Dahele e Ghosh relataram que após a administração oral e parentérica de B12, todos os pacientes ( n = 39) apresentaram níveis séricos normais de B12 no seguimento de um ano [ 67 ]. Um novo papel para a B12 na saúde óssea foi mostrado em um modelo de ratinho de deficiência de B12 demonstrando que a deficiência prejudica a síntese de taurina e melhora a síntese de IGF-1 dependente do hormônio do crescimento no fígado; Isto aumenta a função dos osteoblastos [ 68 ]. A pesquisa em seres humanos deve se concentrar na reavaliação dos requisitos de vitamina B12 na doença celíaca para determinar seu papel na remineralização óssea.
4. Discussão
Nossa compreensão do metabolismo mineral ósseo e do impacto da dieta e do exercício no tratamento da perda mineral óssea para pessoas com doença celíaca está incompleta. Para essa revisão, o autor identificou obras publicadas e a maioria destes foram pequenos ensaios clínicos não aleatorizados. Como a maioria dos participantes foi recrutada em hospitais universitários e centros de tratamento especializado, os resultados podem estar sujeitos a viés de amostragem. Apesar de uma busca exaustiva, apenas dois estudos foram encontrados usando o controle randomizado, e estes não usaram uma análise de intenção de tratar, apesar do desgaste do assunto. Os estudos também não possuíam uniformidade nas medidas de ingestão dietética e avaliação de conformidade. É fundamental desenvolver um banco de dados de dados brutos individuais de estudos sobre densidade óssea e doença celíaca para que uma meta-análise de dados de participantes individuais possa ser publicada [ 79 ]. Este tipo de análise pode diferenciar os efeitos do tratamento para diferentes subgrupos, como não respondedores. A incidência de DC continua a crescer em todos os grupos etários, criando necessidade de melhor gerenciamento da baixa DMO em adultos e idosos [ 80 ].
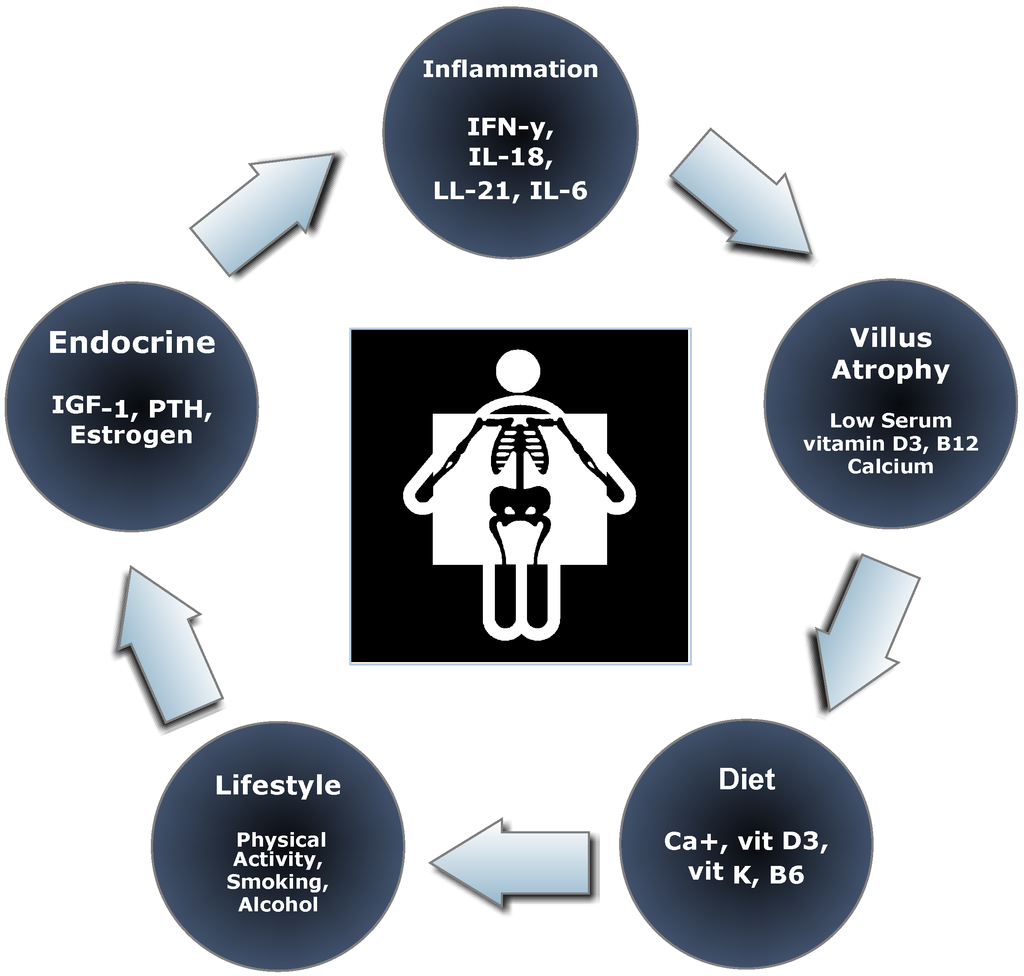
É pensada que a má absorção de nutrientes devido à inflamação crônica e à atrofia das vilosidades são as principais causas de baixa DMO ( Figura 2 ). No osso, o cálcio é regulado pelo hormônio paratireoidiano (PTH), 1,25-dihidroxivitamina D (vitamina D3) e calcitonina [ 81 ]. O hiperparatiroidismo é comum na doença celíaca não tratada e é caracterizado por alta rotatividade óssea e perda óssea cortical [ 82 ]. Além disso, alterações na função da vesícula biliar, insuficiência pancreática exócrina e permeabilidade intestinal reduzem a absorção de nutrientes essenciais [ 83 ]. A DMO está diretamente relacionada à extensão da atrofia das vilosidades, o que resulta em má absorção de cálcio, ferro, vitamina D e ácido fólico [ 84 ]. Mesmo após muito tempo após o início do tratamento dietético, a absorção de cálcio pode ser reduzida [ 85 ]. Quando administrado com vitamina D, a Vitamina K demonstrou aumentar a DMO na osteoporose e reduzir as taxas de fratura devido ao seu papel no equilíbrio de cálcio [ 86 ].
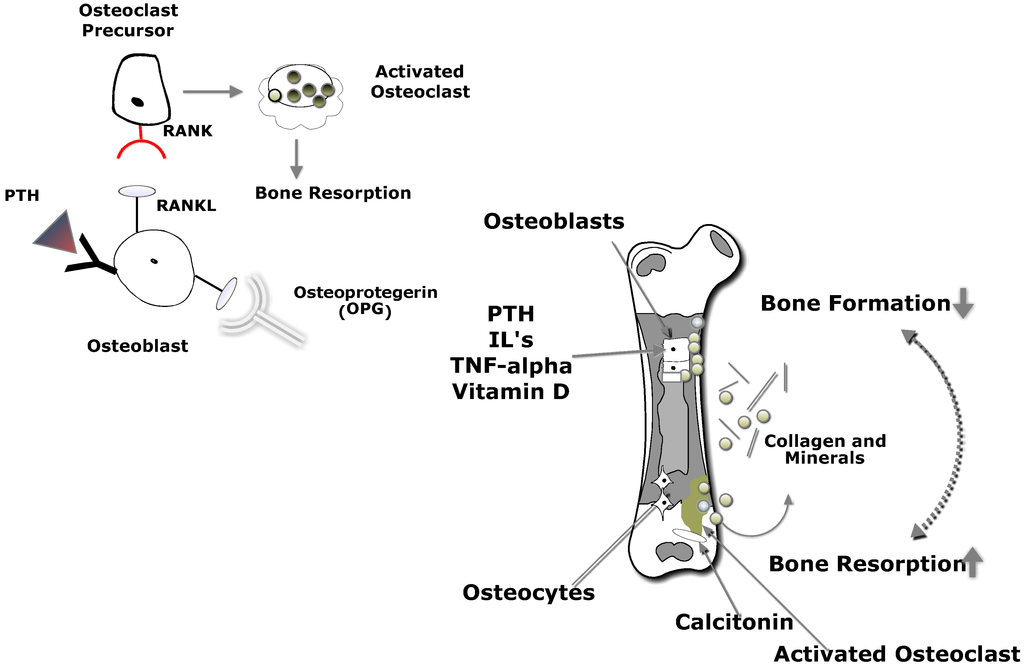
O osso é tecido dinâmico que está passando continuamente através da reabsorção e absorção de cálcio de sangue para osso em um processo chamado remodelação ( Figura 3 ). A perda de densidade óssea no CD é causada por um desequilíbrio na osteoclastogênese e na atividade dos osteoblastos, conforme relatado em um estudo sobre pacientes recém-diagnosticados em comparação com indivíduos em um GFD [ 30 ]. Os autores relataram que os fatores pró-inflamatórios, o telopeptídeo N- terminal de procollagen tipo I e IL-6, foram maiores no grupo CD não tratado, sugerindo que os fatores reguladores do turnover ósseo contribuíram para a redução da massa óssea.Outros fatores inflamatórios envolvidos na patogênese do metabolismo ósseo são a osteoprotegerina (OPG), um membro da família do receptor do fator de necrose tumoral e RANKL. RANKL é uma citocina que estimula a formação e ativação dos osteoclastos no osso, enquanto o OPG atua como um receptor de chamariz para RANKL, controlando assim sua função. A relação OPG / RANKL foi significativamente menor em pacientes com CD em um estudo controlado de mulheres pré-menopáusicas do que em controles pareados com idade, e a relação OPG / RANKL foi correlacionada com a perda de DMO na coluna vertebral [ 44 ]. Fatores demográficos e de estilo de vida como idade, gênero, distúrbios alimentares, abuso de álcool, baixa atividade física e tabagismo também estão associados a baixa DMO no CD [ 55 , 80 , 87 ].
Figura 3. Remodelação óssea. À medida que os níveis de PTH aumentam, osteoblastos regulam a expressão de RANKL, que se liga ao RANK, ativando vias de sinalização que promovem a diferenciação dos osteoclastos. Osteoblastos secretam osteoprotegerina que protege os ossos da reabsorção. A osteoprotegerina se liga ao RANKL e evita a ligação ao RANK, portanto, a estimulação da frequência da osteoclastogênese é reduzida. PTH: hormônio paratiroideiro; RANK: ativador receptor de fator nuclear-κB; RANKL: ativador do receptor do fator nuclear -kB ligando.
5. Conclusões
O comportamento mais importante que afeta a densidade óssea na doença celíaca é a aderência à dieta. Os determinantes psicológicos da aderência à GFD, como autodisciplina, valores, depressão, ansiedade e presença de outras intolerâncias alimentares podem ter um efeito na reabilitação óssea [ 88 ]. Pacientes que lutam com personalidade e barreiras psicológicas para a conformidade com a dieta podem se beneficiar de técnicas de entrevista motivacional no início do tratamento [ 89 ]. Os adultos diagnosticados com doença celíaca podem ter uma má absorção de longa data, portanto, podem se beneficiar de terapia de ferro, folato, B12, vitamina D3, vitamina K, cálcio, magnésio e ácido docosahexaenóico (DHA) [ 66 , 77 , 90 ]. As deficiências da densidade de nutrientes da dieta isenta de glúten exigem os serviços iniciais e individualizados de um nutricionista-nutricionista registrado com conhecimentos de doença celíaca em terapia de nutrição médica e coaching de estilo de vida [ 91 ].
Reconhecimentos
O autor quer agradecer aos colegas da Coorte da Promoção da Saúde e do Bem-Estar na Rocky Mountain University of Health Professions, especialistas em áreas de nutrição, fisioterapia, terapia ocupacional ou treinamento atlético, por me fornecer críticas construtivas que influenciaram os rascunhos iniciais Deste manuscrito. O autor agradece a assistência de Teresa E. Araas, que revisou críticamente as revisões subseqüentes.
Conflitos de interesse
O autor declara nenhum conflito de interesse.



Comentários
Postar um comentário